Tính ổn định của dung dịch SnSO4, H2SO4
06/12/2017
Việc nghiên cứu tìm ra các chất phụ gia làm ổn định dung dịch điện phân có ý nghĩa rất lớn trong công nghiệp tinh luyện lấy thiếc sạch bằng phương pháp điện phân trong dung dịch SnSO4-H2SO4 của nước ta.
Stability of the solution SnSO4, H2SO4
TS Đinh Tiến Thịnh Trường Đại học Bách khoa Hà Nội
TÓM TẮT
Tính ổn định của dung dịch là một yếu tố quan trọng khi tiến hành điện phân, nó ảnh hưởng rất nhiều đến chất lượng kết tủa catốt. Việc nghiên cứu tìm ra các chất phụ gia làm ổn định dung dịch điện phân có ý nghĩa rất lớn trong công nghiệp tinh luyện lấy thiếc sạch bằng phương pháp điện phân trong dung dịch SnSO4-H2SO4 của nước ta.
ABSTRACT
Stability of the solution is an important factor when conducting electrolyte, which affects many quality cathode deposition. Some additives are found to stabilize the liquid electrolyte. It is essential for the refining industry, where pure tin is extracted by the electrolytic method in solution SnSO4-H2SO4.
1. Đặt vấn đề
Hiện nay công suất các cơ sở điện phân tinh luyện thiếc trong nước đã sản xuất được trên 2000 tấn thiếc sạch/năm. Lượng thiếc này có thể cung cấp đủ nhu cầu thiếc sạch trong nước và mang lại lợi ích không nhỏ do tiết kiệm được ngoại tệ dùng cho việc nhập khẩu. Nguyên liệu đầu vào tại các cơ sở tinh luyện thường là các loại thiếc thô còn chứa nhiều các tạp khó xử lý như chì, bitmut... sau quá trình hỏa luyện.
Do tính không ổn định trong khai thác cùng lợi nhuận khá lớn của quả trình điện phân tinh luyện nên các cơ sở sản xuất đua nhau phát triển, dẫn tới hiện tượng mất cân đối lượng thiếc thô cung cấp, nhiều bể điện phân làm việc một thời gian lại phải ngừng cấp điện. Đặc tính của các iôn thiếc tồn tại trong axit sun- fuaric là ở 2 dạng iôn Sn2+ và Sn4+ [1].
Trong quá trình tiếp xúc với không khí, iôn Sn2+ dễ bị ôxy hóa tạo Sn4+. Nồng độ bão hòa của Sn4+ khá nhỏ nên rất dễ bị thủy phân tạo kết tủa SnO2 [2]. Trong quá trình điện phân, Sn4+ ưu tiên phóng điện và duy trì một hàm lượng cân bằng với Sn2+ trong dung dịch. Khi ngừng cấp điện, Sn4+ tích lũy dần dẫn đến thủy phân làm giảm hàm lượng thiếc trong dung dịch, gây khó khăn lớn cho quá trình khới động lại bể và sản xuất tiếp theo.
Thực tế này đang xảy ra tại các cơ sở điện phân trong nước, đó là khi đóng điện trở lại, thường phải mất từ 1 đến 3 ngày để ổn định lại dung dịch, gây tiêu tốn điện năng cùng với đó kết tủa nhánh cây ở catốt. Trước tình hình này, việc nghiên cứu tìm ra thành phần dung dịch thích hợp với các phụ gia làm kìm hãm quá trình ôxy hóa Sn2+ thành Sn4+, giảm thiểu lượng SnO2 bị kết tủa, duy trì nồng độ thiếc ổn định trong dung dịch có một ý nghĩa rất to lớn.
2. Thực nghiệm
Nội dung nghiên cứu gồm 3 phần:
- Nghiên cứu cặn kết tủa của dung dịch điện phân khi để trong môi trường không khí.
- Nghiên cứu ảnh hưởng của nồng độ axit H2SO4 đến tính an toàn của dung dịch. Dung dịch ban đầu được chọn với nồng độ ion thiếc tổng là: 34.4 g/l, nồng độ axit H2SO4 thay đổi lần lượt là 80, 100, 120, 140 g/l được chọn để nghiên cứu.
- Nghiên cứu ảnh hưởng của các phụ gia đển tính an toàn của dung dịch.
Kết quả nghiên cứu của phần 1 là cơ sở để chọn nồng độ axit cho nghiên cứu tiếp theo: 120 g/l axit H2SO4; 34.4 g/l SnΣ. Các phụ gia sau đây được chọn làm đối tượng nghiên cứu gồm: β-napton; Cl - ; Cr 6+; Gelatin + β- napton và Cr 6+ + Cl - , đó chính là các chất thường được pha vào dung dịch điện phân và các phụ gia có ảnh hưởng quyết định đển chu kỳ anôt [2].
Mỗi loại dung dịch đều được chuẩn bị với lượng như nhau, được đổ vào các bình tam giác giống nhau, theo rõi và phân tích hàm lượng Sn tổng theo thời gian, cụ thể sau 8; 15; 25 ngày.
3. Kết quả và thảo luận
3.1. Nghiên cứu cặn kết tủa của hệ dung dịch SnSO4-H2SO4
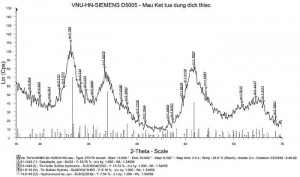
Dung dịch điện phân sau thời gian để tự nhiên trong không khí 01 tuần, lọc lấy kết tủa đưa đi phân tích X-ray. Kết quả được thể hiện trên hình 1.
Hình 1. Giản đồ nhiễu xạ rơngen của dung dịch điện phân sau 1 tuần trong không khí
Kết quả phân tich X-ray cho thấy thành phần kết tủa chủ yếu là SnO2, chứng tỏ iôn Sn2+ đã bị ôxy hóa thành iôn Sn4+ rồi dần dần bị thủy phân thành SnO2.
3.2. Ảnh hưởng của nồng độ axit
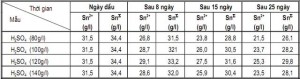
Pha cùng lúc một loạt các bình thủy tinh cùng thể tích, với hàm lượng iôn thiếc ban đầu như nhau nhưng khác nhau về nồng độ axit. Phân tích sự thay đổi nồng độ iôn thiếc theo thời gian. ảnh hưởng nồng độ axit H2SO4 và thời gian đến tính an toàn của dung dịch được ghi trong bảng 1 và thể hiện trên đồ thị hình 2.
Bảng 1. Hàm lượng iôn thiếc thay đổi theo nồng độ axit và thời gian
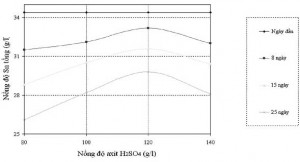
Hình 2. Quan hệ giữa nồng độ Sn tổng với nồng độ axit H2SO4 và thời gian
Nhận xét:
- Ảnh hưởng của thời gian. Trong dung dịch axit H2SO4 thuần (không có phụ gia) cho thấy ở tất cả các thành phần axit được nghiên cứu, nồng độ Sn tổng đều giảm theo thời gian. Cùng với hàm lựợng Sn giảm, lượng kết tủa màu ngà vàng cũng tăng lên. Điều này đã khẳng định rằng theo thời gian Sn2+ bị ôxy hóa tạo Sn4+ và kết tủa.
- Ảnh hưởng của nồng độ axit. Trong khoảng nồng độ axit từ 80 g/l đến 120 g/l với cùng một thời gian như nhau dung dịch có nồng độ axit càng lớn nồng độ thiếc tổng duy trì được càng lớn. Khi nồng độ axit vượt quá 120 g/l lên 140 g/l nồng độ thiếc lại giảm, mức độ duy trì tương đương nồng độ axit 100 g/l.
Như vậy, nồng độ 120 g/l axit H2SO4 có tính ổn định dung dịch cao nhất.
3.2. Ảnh hưởng của các chất phụ gia
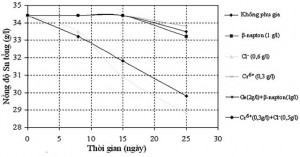
Ảnh hưởng của các chất phụ gia đến độ an toàn của dung dịch điện phân thiếc ghi lại trong bảng 2 và mô tả trên đồ thị hình 3.
Bảng 2. Hàm lượng iôn thiếc thay đổi theo chất phụ gia và thời gian
Hình 3. Quan hệ giữa nồng độ Sn tổng với nồng độ các chất phụ gia và thời gian
Nhận xét
- Các chất có ảnh hưởng xấu đến độ an toàn dung dịch. Dung dịch điện phân thiếc H2SO4-SnSO4 thuần, khi không điện phân (ngừng đóng điện), nồng độ thiếc tổng ban đầu là 34.4 g/l, sau 25 ngày nồng độ Sn tổng giảm xuống còn 29,8 g/l, tức là giảm 13,4% (đường không phụ gia - hình 3). Khi cho lượng ion Cl - là 0.6 g/l vào dung dịch, sau 25 ngày, lượng Sn tổng giảm từ 34.4 g/l (ngày đầu) xuống còn 28,8 g/l tức là giảm 16,3%.
Như vậy, trong số 5 loại phụ gia đã áp dụng vào nghiên cứu ảnh hưởng tới độ an toàn dung dịch điện phân cho thấy, ion Cl - có ảnh hưởng xấu nhất, tồi tệ hơn cả khi không có một loại phụ gia nào. Nồng độ Sn trong dung dịch giảm mạnh theo thời gian, lượng kết tủa sinh ra ở đáy bình cũng nhiều nhất, nhiều hơn cả trường hợp không có phụ gia.
- Các chất có tác dụng ổn định dung dịch. Đối với các chất phụ gia còn lại như: β-napton (1 g/l); Cl - (0,6 g/l); Cr 6+ (0,3 g/l); Gelatin (2 g/l) + β-napton (1 g/l); Cr 6+ (0,3 g/l) + Cl - (0,5 g/l) đều có tác dụng ổn định dung dịch khá tốt. Trong 15 ngày đâu, nồng độ thiếc tổng trong dung dịch hầu như không giảm. Đến ngày thứ 25, các phụ gia β-napton và gelatin không duy trì được nồng độ thiếc tổng ban đầu nữa, đã giảm đi 3,4% (xuống 33,2 g/l). Iôn Cr có tác dụng duy trì độ ổn định của dung dịch tốt nhất. Khi có thêm iôn Cl, độ ổn định có giảm đôi chút, song không đáng kể.
4. Kết luận
Tính ổn định của dung dịch phụ thuộc vào nhiều yếu tố, ở đây mới đề cập đến: nồng độ axit tổng và các chất phụ gia cho thêm vào dung dịch. Nồng độ axit tổng 120 g/l cho kết quả tốt nhất, song với nồng độ trong khoảng 100 g/l đến 140 g/l vẫn có thể chấp nhận được trong sản xuất. Các chất phụ gia cho vào để kéo dài chu kỳ anôt như các ôn Cl, Cr [2] có tác dụng trái ngược nhau. Trong khi iôn Cr có tác dụng ổn định dung dịch điện phân rất tốt thì sự có mặt của iôn Cl làm cho quá trình ôxy hóa thiếc 2 xảy ra nhanh hơn, dẫn đến nồng độ thiếc trong dung dịch giảm mạnh. Sự có mặt đồng thời của cả hai iôn Cr và Cl đã làm yếu đi khả năng ôxy hóa của Cl, vừa có tác dụng kéo dài thời gian thụ động anôt đồng thời vẫn đảm bảo được tính ổn định của dung dịch khá tốt.
[symple_box color="blue" text_align="left" width="100%" float="none"]
Tài liệu trích dẫn
- Đinh Phạm Thái, Nguyễn Kim Thiết, Lý thuyết các quá trình luyện kim - Điện phân, NXB Giáo dục, Hà Nội 1997.
- Đinh Tiến Thịnh, Tối ưu hóa quá trình anôt điện phân tinh luyện thiếc trong dung dịch sunfat, Luận án tiến sĩ, Bộ Giáo dục và Đào tạo, Hà Nội, 2008
[/symple_box][symple_clear_floats]